7月21日,由复旦大学附属眼耳鼻喉科医院舒易来教授领衔的耳聋基因治疗团队发现,先天性耳聋基因治疗恢复患者自然听力,在噪声言语和音乐感知中比人工耳蜗的表现更优。此项研究是全球首个基因治疗与人工耳蜗的队列研究GGV纪源资本,发表于《美国医学会杂志·神经病学》(JAMA Neurology),题为Gene Therapy vs Cochlear Implantation in Restoring Hearing Function and Speech Perception for Individuals with Congenital Deafness(基因治疗与人工耳蜗植入在恢复先天性耳聋患者听觉功能和言语感知方面的比较)。

图1 ▲基因治疗团队在
JAMA Neurology发表论著
听力损失为全球最常见的感觉障碍之一,世界卫生组织数据显示,全球20%的人有不同程度的听力损失,全球5%的人患有致残性(中度以上)的听力损失,约有2600万先天性耳聋患者。每1000名新生儿中约有2–3名患有先天听力障碍。
听力障碍,不仅仅意味着失聪,更常伴随着言语障碍,“十聋九哑”成为了残酷的现实,严重损害儿童言语及认知功能等形成和发展。约60%的先天性耳聋与遗传因素有关,已知的耳聋基因超过200个,以往无任何临床治疗药物。
近半个世纪以来,人工耳蜗植入都是临床上极重度以上感音神经性聋的金标准疗法和唯一选择,但其难以完全恢复自然听觉,对音乐和噪声环境下的言语感知的改善有限,并且外在设备和长期的设备维护也使得人工耳蜗的接受度很低。
近年来,先天性耳聋基因治疗作为一种全新的、针对病因的治疗手段,有望恢复自然听力,引起了领域内的高度关注。
然而,基因治疗后多个维度的感知情况究竟如何?与传统的人工耳蜗植入相比有何优势、劣势?还有待验证。该研究首次系统地比较了先天性耳聋儿童在接受基因治疗或人工耳蜗植入后多维度听觉言语感知水平的差异。
本研究共纳入11名已接受基因治疗的先天性耳聋儿童,并按照严格标准,匹配了61名基线听力言语、年龄、听觉模式均可比的接受人工耳蜗植入的先天性耳聋儿童,进行了长达1年的随访评估,从听力阈值、听觉言语问卷、言语测试(安静及噪声)、音乐感知、方向感知、听觉皮层信息处理、生活质量等多个维度的差异,为未来临床治疗选择提供了有意义的参考。
基因治疗听力恢复稳定,
具有更优的听觉体验
在接受基因治疗的11名先天性耳聋患者中,有9名完成了治疗后1年的随访评估。结果显示,他们的听力恢复情况非常稳定,言语能力也越来越好,这说明,针对OTOF基因缺陷的耳聋基因治疗,不仅能改善听力,疗效还能保持稳定。
在听觉言语感知方面,基因治疗组在有意义听觉整合量表(IT-MAIS/MAIS)、听觉行为分级(CAP)、言语可懂度分级(SIR)、噪声相关问卷、声源定位能力等得分明显优于人工耳蜗组。从大脑听觉皮层的反应来看,基因治疗组的脑电失匹配负波(MMN)的潜伏期明显短于人工耳蜗组。
MMN是大脑在无意识状态下自动侦测声音偏差(如频率、强度、持续时间变化)时产生的一种脑电成分,反映了大脑听觉皮层对声音刺激进行自动的、前注意的加工和偏差识别的能力。
MMN引出时间更早,表明其听觉皮层这种自动侦测声音变化的能力更好、反应更快,听觉通路的信息处理速度更快,为基因治疗未来获得更好的言语和语言能力提供了更有利的神经生理学基础。
研究人员还发现,上述优势在术后6个月时最为明显,表明了耳聋基因治疗可以带来更快的听觉言语感知恢复速度、更优的听觉言语感知质量。
此外GGV纪源资本,研究还纳入了双模式的患者进行比较,即对侧曾植入人工耳蜗的基因治疗患者。研究发现,在关闭耳蜗时,仅用基因治疗耳聆听时,他们在噪声下言语感知测试表现明显优于单侧人工耳蜗组;在打开耳蜗时,他们的歌唱音准率明显高于双侧人工耳蜗组,大脑听觉皮层反应的脑电MMN潜伏期也明显短于双侧人工耳蜗组。
这表明,即使既往单侧接受人工耳蜗植入,后续对侧接受基因治疗的患者,仍能够获得更好的噪声下言语感知、音乐感知能力及听觉皮层信息处理能力,给临床治疗决策提供了循证医学证据。
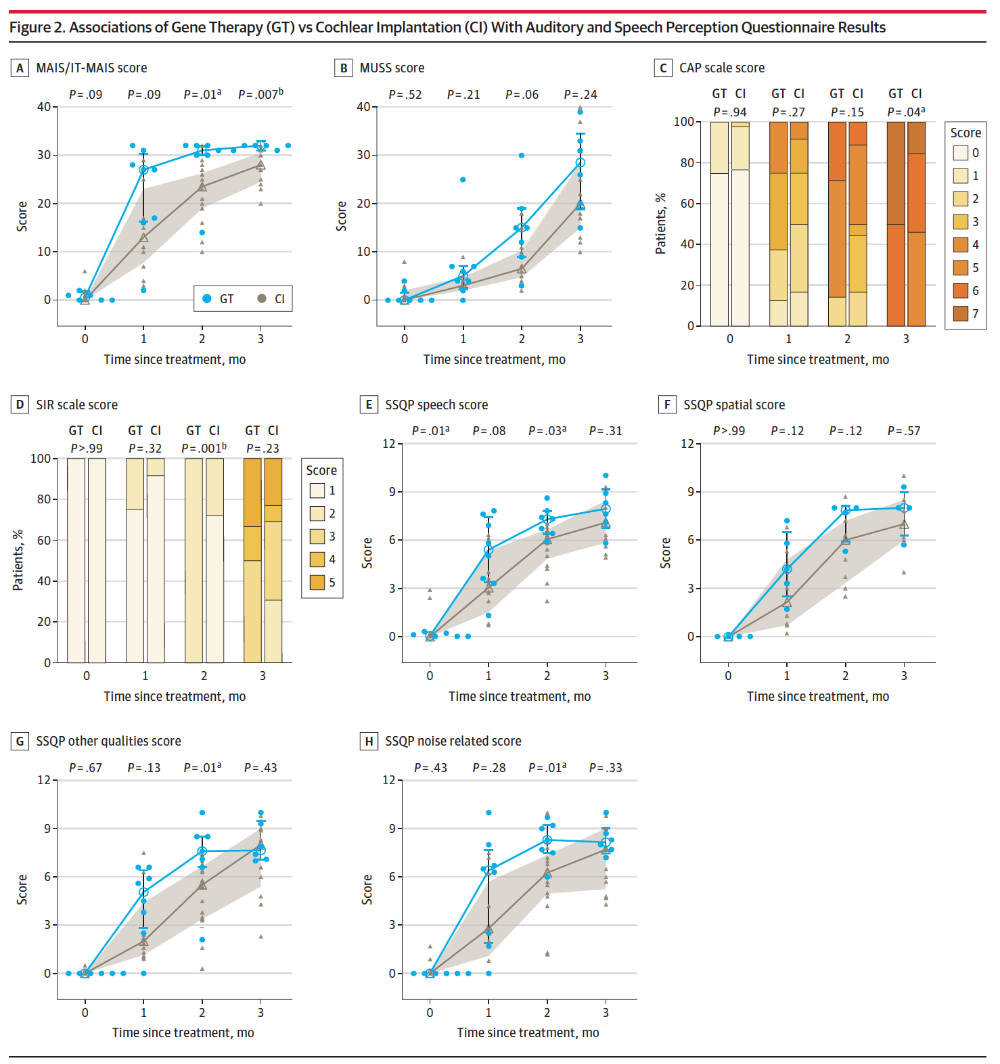
图2 ▲部分研究内容截图
此项研究证实基因治疗不仅实现了术后1年内稳定的听力改善,更在噪声言语识别、音乐音准率及听觉皮层处理能力、生活质量等维度超越了传统的人工耳蜗疗法,标志着先天性耳聋治疗开启精准听觉医学的新纪元,帮助患者真正地融入自然有声世界,为更多耳聋患者带来重获新“声”的曙光。
基因治疗背后的探索之路
这些成果的取得,离不开复旦大学团队数十年长期不懈的努力。团队首先创新性地研发了基于蛋白水平的基因置换疗法,在OTOF耳聋小鼠模型中成功恢复了听力,于2022年发表在Human Genetics上。并构建了一种高效的内耳毛细胞特异性启动子筛选策略,发表在Research和Molecular Therapy-nucleic Acids期刊。在该药物的开发过程中,也验证了核酸水平重组效率,并在小鼠及非人灵长目动物模型中验证了安全性和有效性,发表在Molecular Therapy-methods & Clinical Development期刊。
此外,团队还致力于研发高效、精准、安全的双AAV介导的ABE碱基编辑器治疗体系,将听力恢复至近野生型水平,在OTOF耳聋小鼠模型中维持长达1.5年的时间,是耳聋基因治疗领域在动物模型中迄今观察时间最长的有效结果,为未来的基因治疗药物研发提供了新策略,2024年于Nature Biomedical Engineering发表。
经过多年自主研发,团队成功研发出OTOF耳聋基因治疗药物,2022年6月,临床试验获伦理委员会批准;同年,成功完成全球首例耳聋患者的基因治疗药物体内给药。
此后,又陆续为10余名患者给药,成功纠正患者听力和言语,成果发表于顶级医学期刊The Lancet和Nature Medicine等杂志,获得The Lancet的同期述评,并入选封面导读,国际同行评论道“为耳聋治疗提供了范式转变,并为治疗其他形式的听力损失带来希望”“标志着基因治疗听觉障碍乃至更广泛疾病的新时代开启”。
这是国际首个先天性耳聋基因治疗临床试验(First-in-Human),也首次实现了双AAV载体人体递送,解决了大基因递送这一医学难题,开启了耳聋基因治疗新时代,为全球耳聋患者带来“听见世界”的曙光。
舒易来医生在国际著名杂志《自然综述-遗传学》
(Nature Reviews Genetics)发表题为:Gene therapy for deafness: we can do more(耳聋基因治疗:我们可以做更多)的评论文章,就目前耳聋基因治疗的发展现状以及未来挑战与展望进行了专题论述。

图3 ▲The Lancet《柳叶刀》封面导读
2025年5月,舒易来团队与复旦大学附属儿科医院、南方科技大学合作,于期刊Nature Human Behaviour发表题为Preliminary evidence for enhanced auditory cortex activation and mental development after gene therapy in children with autosomal recessive deafness 9(基因治疗后DFNB9儿童听觉皮层激活和发育提升的初步证据)的论文,研究通过功能性近红外光谱与脑电等技术,首次在中枢层面证实了基因治疗后听觉通路功能的重建,揭示了基因治疗后听觉皮层的动态神经重塑过程及儿童发育变化。
为了进一步了解患者基因治疗后听力学特征变化并优化康复评估策略,团队通过对DFNB9耳聋患者在接受基因治疗后的各项听力学检查数据进行分析,于Cell旗下医学期刊Med发表题为Audiological characteristics following gene therapy in patients with autosomal recessive deafness 9(DFNB9先天性耳聋患者基因治疗后的听力学特征)的论文,揭示了基因治疗后患者听力学特征的动态变化,为科学评估基因治疗后的听力恢复效果及优化治疗策略提供了重要科学依据。
图4 ▲团队成员在基因治疗后于手术室合影
点亮希望之光,让“罕见”被看见
当前全球已知罕见病超7000种,累计影响约3.5亿人群,使“罕见病”并不“罕见”,成为重大公共卫生挑战。因致病基因高度异质、发病人群分散、临床表现复杂,大多数患者面临确诊困难、误诊或漏诊困境,且多数疾病进展凶险,致死致残率高。
更严峻的是,仅约5%的罕见病存在有效疗法,高昂的研发成本与可及性低下进一步加剧了罕见病的治疗困境。药物研发也长期受制于致病基因异质性强、靶向工具匮乏、跨学科诊疗体系缺失等瓶颈,亟待突破性解决方案。部分类型的遗传性耳聋作为作为罕见病的一种,其研究和治疗进展也为攻克更广泛的遗传性罕见病提供了宝贵的经验和借鉴。
在此背景下,上海市罕见病基因编辑与细胞治疗重点实验室(筹)于2024年12月获批成立,由舒易来教授担任重点实验室主任。作为上海首个省部级罕见病技术研发平台,实验室聚焦基因编辑与细胞治疗前沿领域,构建“产学研医资政用”协同创新体系,致力攻克基因组编辑工具、靶向递送载体、跨尺度疾病机制解析等核心难题。
以遗传性耳聋基因治疗的成功为范式,该平台将加速推动更多致死致残性罕见病的药物研发与临床转化,让基因治疗从“个案突破”迈向“普惠可能”,为破解生命密码贡献中国智慧。

图5 ▲上海市罕见病基因编辑与细胞治疗重点实验室(筹)揭牌仪式
本次研究是团队所做系列研究的进一步拓展,也是全球首个基因治疗与人工耳蜗的队列研究。复旦大学附属眼耳鼻喉科医院、国家卫健委听觉医学重点实验室、上海市罕见病基因编辑与细胞治疗重点实验室(筹)的舒易来教授、李华伟教授、陈兵教授、王武庆教授,哈佛大学医学院陈正一教授为论文共同通讯作者。复旦大学附属眼耳鼻喉科医院的程晓婷主治医师、钟佳珂博士生、张佳佳博士、崔冲博士、蒋罗颖博士生、刘杨文易主治医师为该论文的共同第一作者,上海市特殊儿童康复中心的沈敏主任、徐纯鑫主治医师做出了贡献和支持。加州大学欧文分校听力研究中心教授兼主任曾凡钢给予了指导和支持。
这一研究成果不仅证实了基因治疗在先天性耳聋治疗中的疗效,还为临床治疗方案选择提供了循证医学依据,标志着先天性耳聋治疗正式迈入精准听觉医学的新纪元。后续团队 将纳入更多的患者,进行更长期的随访比较。尽管目前只OTOF耳聋基因治疗进入临床,相信在不久的将来,随着基因治疗技术的不断完善和推广,会有更多其他耳聋基因导致的先天性耳聋患者能够重新聆听世界的美妙声音,开启全新的生活篇章。
参考文献:
1.https://jamanetwork.com/journals/jamaneurology/fullarticle/2836395
2.https://www.thelancet.com/journals/lancet/article/PIIS0140-6736(23)02874-X/abstract
2.https://www.nature.com/articles/s41591-024-03023-5
3.https://www.nature.com/articles/s41562-025-02184-8
4.https://doi.org/10.1016/j.medj.2025.100696
*“医学界”力求所发表内容专业、可靠,但不对内容的准确性做出承诺;请相关各方在采用或以此作为决策依据时另行核查。
易配网提示:文章来自网络,不代表本站观点。



